NAD+前駆体とエクソソーム療法は、いずれも再生医療の臨床医から真剣な注目を集めています。どちらも生物学的根拠があり、エビデンスも蓄積されつつあり、測定可能な抗老化効果を求める患者に提供されています。しかし、両者は根本的に異なるメカニズムで作用し、異なるタイムスケールで機能し、エピゲノムに異なる痕跡を残します。精密な長寿プロトコルを構築するすべての医師にとって、この違いを理解することは不可欠です。
本稿では、各介入の科学的根拠を検討し、臨床エビデンスを比較し、どちらが実際に効果をもたらしているか——そしていつ効果が現れるか——を客観的に判断できる唯一のツールであるDNAメチル化スクリーニングについて解説します。
両介入が解決しようとしている問題
人体のすべての細胞は老化します。ミトコンドリアは効率を失い、DNA修復は誤りを起こしやすくなり、炎症シグナルは増大し、組織再生は遅くなります。これらは独立した障害ではなく、単一の根本的な変化——エピゲノムの進行性の調節不全——の相互に連関した結果です。
DNAメチル化、すなわちゲノム全体のCpGサイトにおけるシトシン塩基の化学的修飾は、この調節不全の最も安定した測定可能な記録の一つです。ゲノム全体のメチル化データで訓練された数学的モデルであるエピジェネティック時計は、生物学的年齢を驚くほど正確に推定できます。介入が細胞の老化を真に逆転させると、メチル化パターンが変化します。そうでない場合、患者がどのように感じていても、時計は刻み続けます。これがNAD+とエクソソームを評価する視点です。
NAD+:エンジンへの燃料補給——再構築ではない
メカニズム
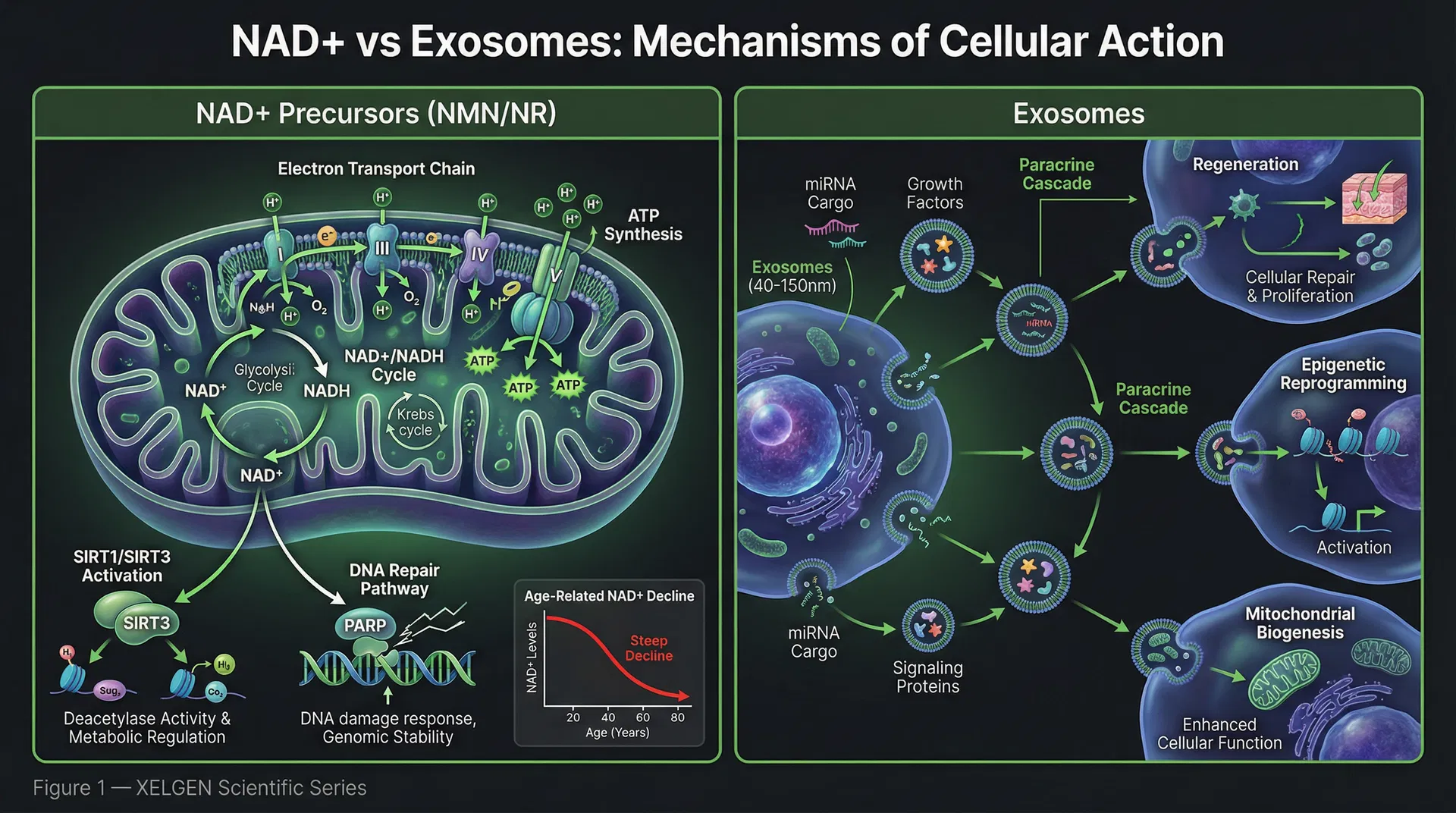
ニコチンアミドアデニンジヌクレオチド(NAD+)はすべての細胞に存在する補酵素であり、ミトコンドリアのエネルギー産生に不可欠です。電子伝達系では、NADHが電子を供与してATP合成を駆動します——これが細胞活動の生化学的通貨です。エネルギー代謝を超えて、NAD+は細胞の健康と長寿を直接支配する2つの酵素ファミリーの必須基質として機能します:サーチュイン(SIRT1〜SIRT7)とポリ(ADP-リボース)ポリメラーゼ(PARP)です。
サーチュインはNAD+依存性脱アセチル化酵素です。このファミリーのミトコンドリア関連メンバーであるSIRT1とSIRT3は、ミトコンドリア生合成、酸化的リン酸化効率、および抗酸化防御を調節します。NAD+が豊富な場合、サーチュインは活性化され、細胞は代謝の規律を維持します。NAD+が不足すると、サーチュイン活性が崩壊し、ミトコンドリアの品質管理が低下し、細胞は老化の特徴を蓄積し始めます。
PARPはDNA鎖切断を修復するためにNAD+を消費します。酸化ストレス、UV曝露、複製エラーによるDNA損傷が年齢とともに蓄積するにつれ、PARP活性が増大し、NAD+を加速度的に消費します。これにより悪循環が生じます:より多くの損傷がより多くのNAD+修復を必要とし、そもそも損傷を防ぐサーチュインに利用可能なNAD+が減少します。
NAD+が年齢とともに減少する理由
細胞内NAD+の加齢に伴う減少は十分に記録されており、少なくとも3つの収束する力によって駆動されます。第一に、免疫細胞と内皮細胞に発現するNAD+加水分解酵素CD38は、加齢とともに活性が劇的に増大します——これは老化した組織を特徴づける慢性的な低グレードの炎症(炎症老化)によって部分的に引き起こされます。第二に、蓄積したDNA損傷に応答したPARPの過活性化が、生合成経路が補充できる速度よりも速くNAD+を消費します。第三に、NAMPTという酵素を介してニコチンアミドをNAD+にリサイクルするNAD+サルベージ経路の効率が加齢とともに低下し、細胞の自己補充能力が低下します。
NMNとNR:基質の補充
ニコチンアミドモノヌクレオチド(NMN)とニコチンアミドリボシド(NR)は、サルベージ経路の律速段階を迂回して細胞内NAD+プールを直接補充するNAD+前駆体です。複数のヒト臨床試験により、両化合物が安全かつ効果的に血液および組織のNAD+濃度を上昇させることが確認されています。NMNは1日900mgまでの用量で忍容性が良好であることが示されており、NRサプリメンテーションは複数の試験コホートで一貫したNAD+上昇を示しています。
下流への影響——改善されたミトコンドリア機能、強化されたサーチュイン活性、より良いDNA修復能力——は生物学的に説得力があります。動物モデルでは、NAD+前駆体サプリメンテーションが老齢マウスの走行持久力を2倍にし、認知機能を改善し、いくつかの老化の代謝マーカーを逆転させました。ヒトのデータはより控えめですが、方向性は一致しており、複数の試験で筋機能、代謝健康、炎症マーカーの改善が報告されています。
⚠ 重要な制限
NAD+は老化した細胞エンジンへの燃料供給を回復させます。エンジン自体を再構築するわけではありません。NAD+が動かしているミトコンドリアは、依然として同じ老化した損傷したミトコンドリアです。数十年にわたって蓄積したエピジェネティックドリフトは、NAD+を回復させても逆転しません。サーチュイン活性はさらなる悪化を遅らせることができますが、メチル化の全体像を若い状態に再プログラムすることはできません。
これは検出タイムラインに直接的な影響を与えます。患者がNMNまたはNRサプリメンテーションを開始しても、エピジェネティック時計——ホルバスの汎組織時計、GrimAge、DunedinPACE——はすぐには変化を記録しません。メチル化の全体像における意味のある測定可能な変化には、何ヶ月もの持続的な介入が必要です。臨床的には、DNAメチル化時計による生物学的年齢の検出可能な変化には、通常6〜10ヶ月の一貫したNAD+前駆体サプリメンテーションが必要であり、それでも変化の大きさは控えめで、食事の質、運動、睡眠、ストレス管理などの生活習慣要因に大きく依存します。
エクソソーム:エンジン自体の再構築
メカニズム
エクソソームは、ほぼすべての細胞タイプから分泌される直径30〜150 nmのナノサイズの細胞外小胞です。それらは生物学的メッセンジャーとして機能し——マイクロRNA(miRNA)、メッセンジャーRNA、タンパク質、脂質、成長因子などの豊富なカーゴをドナー細胞から受容細胞に輸送します。NAD+が既存の細胞機構の基質として作用するのとは異なり、エクソソームは標的細胞の挙動を根本的に変える新しい生物学的指示を届けます。
間葉系幹細胞(MSC)由来のエクソソームは、再生医療で最も臨床的に研究されているクラスです。そのカーゴには通常、TGF-β、VEGF、IGF-1などの成長因子、抗炎症性サイトカイン、および細胞増殖、分化、エピジェネティックリモデリングを支配する遺伝子発現ネットワークを調節する多様なmiRNAレパートリーが含まれます。これらのエクソソームが標的細胞の膜と融合してカーゴを届けると、その効果は単純な代謝ブーストではありません——それは再プログラミングシグナルです。
下流への影響には、ミトコンドリア生合成(新しい健康なミトコンドリアの形成)、炎症促進NF-κBシグナルの抑制、組織修復経路の活性化、そして——重要なことに——エピジェネティックの全体像の直接的な修飾が含まれます。エクソソームのmiRNAは、メチル化コードの分子的な書き手と消し手であるDNAメチルトランスフェラーゼ(DNMT)とテン-イレブン転座(TET)酵素の活性を調節できます。これは、エクソソーム療法がメチル化パターンを若い状態に直接シフトさせる可能性を持つことを意味します。
パラクリンカスケード
単一のエクソソーム治療は単一の細胞に作用するわけではありません。パラクリンカスケード——治療された細胞からその隣接細胞への再生シグナルの伝播——は組織区画全体にわたって効果を増幅します。MSC由来エクソソームを静脈内投与する幹細胞クリニックは、最初に小胞に遭遇する細胞にカーゴを届けるだけではありません——複数の臓器系にわたって再生シグナルを伝播させる生物学的連鎖反応を開始しているのです。この全身的な到達範囲は、エクソソーム治療のエピジェネティックな足跡がNAD+サプリメンテーションよりも早く、より確実に検出できる主な理由です。
エピジェネティック検出タイムライン:臨床的に決定的な違い
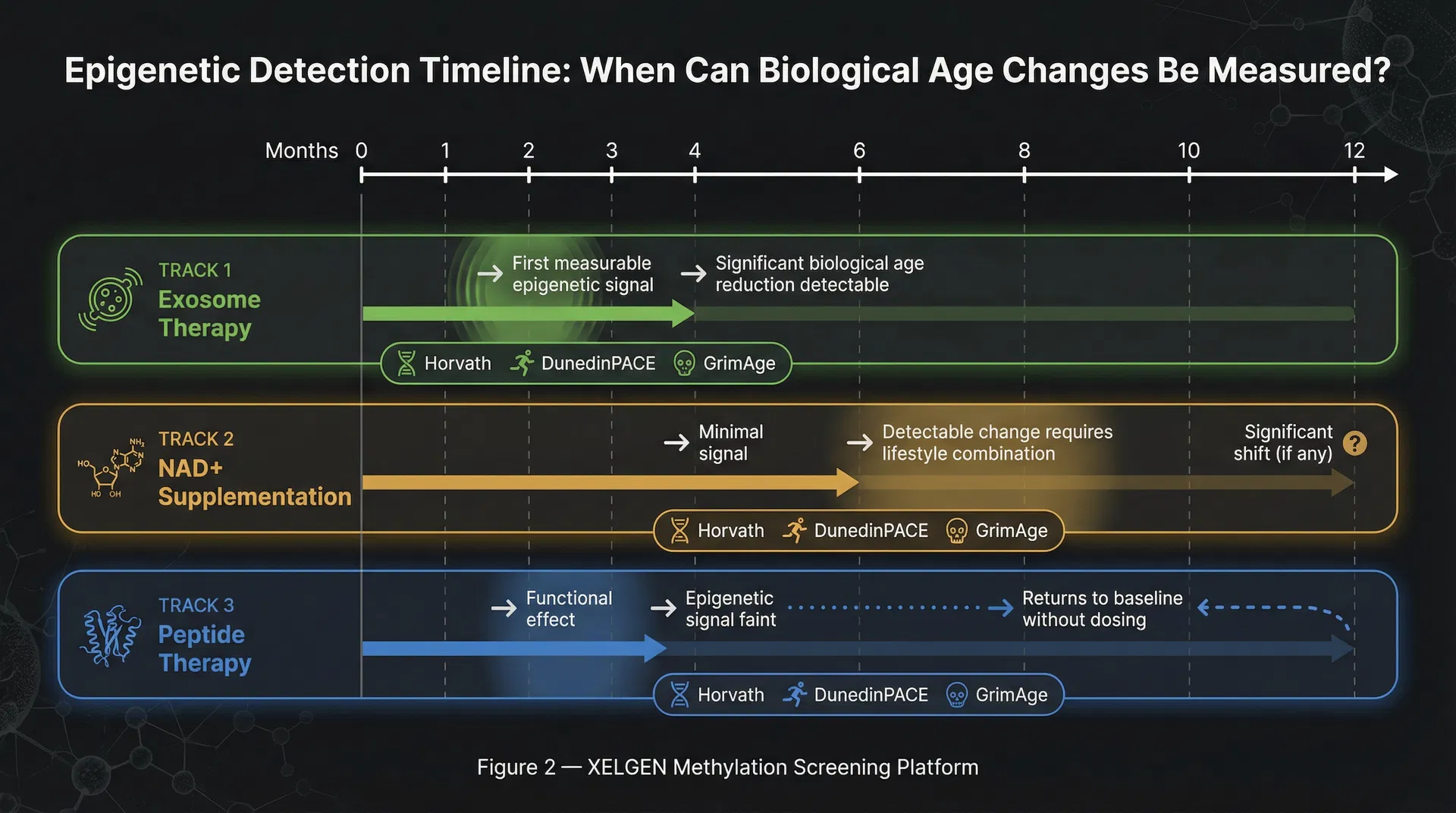
NAD+とエクソソーム療法の最も実際的に重要な違い——臨床医と患者の両方にとって——は、測定可能なエピジェネティックな変化が検出されるタイムラインです。
| 介入 | 最初の検出可能なシグナル | 有意な生物学的年齢変化 | 主要条件 |
|---|---|---|---|
| エクソソーム療法 | 治療後4〜6週 | 3〜4ヶ月 | 用量と製剤品質に依存 |
| NAD+サプリメンテーション | 3〜4ヶ月(最小限) | 6〜10ヶ月(あれば) | 生活習慣の最適化が必要 |
| 併用プロトコル | 4〜6週(エクソソーム主導) | 3〜6ヶ月 | 相乗効果;NAD+は持続的維持をサポート |
エクソソームはmiRNA介在のメチル化酵素調節を通じてエピゲノムに直接作用します。検証済みのメチル化時計(ホルバス、GrimAge、DunedinPACE)での最初の測定可能なシグナルは、通常エクソソーム投与後4〜6週以内に検出できます。臨床的に意味のある生物学的年齢の有意な減少は、一般的に3〜4ヶ月以内に検出可能です。
NAD+サプリメンテーションは間接的な経路を通じて作用します。回復したNAD+はより良いサーチュイン機能を可能にし、細胞のエピジェネティックな忠実性を維持する能力を改善します——しかしこれは維持メカニズムであり、再プログラミングメカニズムではありません。任意の検証済みエピジェネティック時計で統計的に意味のある変化が現れるには、食事、運動、睡眠の最適化と組み合わせた6〜10ヶ月の一貫したサプリメンテーションが通常必要です。
XELGENメチル化スクリーニングの役割
NAD+もエクソソーム療法も、客観的な測定フレームワークなしに投与すべきではありません。患者が報告するアウトカム——エネルギーレベル、睡眠の質、主観的な活力——は価値がありますが、臨床的検証には不十分です。エピゲノムは嘘をつきません。
XELGENのゲノム全体DNAメチル化プラットフォームは、Illumina EPICアレイ技術を使用して850,000以上のCpGサイトを分析し、複数の検証済み時計にわたる生物学的年齢推定値を生成します:ホルバスの汎組織時計、GrimAge(死亡リスク予測因子)、DunedinPACE(老化速度の指標)、PhenoAge。このマルチクロックアプローチは、患者が生物学的老化スペクトルのどこに位置するか、そして——重要なことに——その位置が介入に応じてどのように変化するかについての包括的な全体像を提供します。
ベースラインと6ヶ月時点でのXELGENスクリーニングにより、介入が意味のあるエピジェネティック反応を生み出しているかどうかを客観的に判断できます。6ヶ月の一貫したサプリメンテーションと生活習慣最適化後にメチル化時計が変化していない場合、プロトコルを見直す必要があります。
ベースライン、4〜6週、3〜4ヶ月時点でのXELGENスクリーニングにより、エピジェネティック反応の最も早い検出が可能になります——臨床医が治療効果を確認し、用量を調整し、再生医療がますます求める厳密さでアウトカムを文書化できます。
エクソソームとNAD+を組み合わせて使用する場合、XELGENスクリーニングはネットのエピジェネティックアウトカムの唯一の客観的な指標を提供します——シグナルとノイズを分離し、仮定ではなく実際の生物学的年齢データに基づいてプロトコルを最適化できます。
臨床的推奨事項
精密な長寿プロトコルを構築する医師にとって、エビデンスは明確なフレームワークを支持しています。エクソソームが一次再生介入として機能します——MSC由来エクソソームは、NAD+サプリメンテーションでは再現できないパラクリンシグナルカスケードを通じてメチル化の全体像に直接作用し、現在臨床的に利用可能な最も速く最も確実なエピジェネティック反応を提供します。
NAD+前駆体は維持プロトコルとして機能します——1日500〜1000 mgのNMNまたはNRサプリメンテーションは、エクソソーム治療サイクルの間のミトコンドリア機能とサーチュイン活性をサポートします。これはエクソソーム療法の代替ではなく、エクソソームが開始するエピジェネティックな利益を持続させる代謝的基盤です。
「再生医療の未来は介入の選択ではありません——それらを知的に組み合わせ、唯一重要な真実の基準、すなわちエピゲノムが実際に示すものに対して測定されたプロトコルを構築することです。」
XELGENのゲノム全体メチル化プラットフォームは、最初のエクソソーム治療から長期的なNAD+維持まで、すべての介入を検証するための客観的な生物学的年齢データをクリニックに提供します。
プラットフォームアクセスをリクエスト参考文献
- Yoshino, J., Baur, J.A., & Imai, S.I. (2018). NAD+ Intermediates: The Biology and Therapeutic Potential of NMN and NR. Cell Metabolism, 27(3), 513–528. https://doi.org/10.1016/j.cmet.2017.11.002
- Verdin, E. (2015). NAD+ in aging, metabolism, and neurodegeneration. Science, 350(6265), 1208–1213. https://doi.org/10.1126/science.aac4854
- Covarrubias, A.J., et al. (2021). NAD+ metabolism and its roles in cellular processes during ageing. Nature Reviews Molecular Cell Biology, 22(2), 119–141. https://doi.org/10.1038/s41580-020-00313-x
- Yoshino, M., et al. (2021). Nicotinamide mononucleotide increases muscle insulin sensitivity in prediabetic women. Science, 372(6547), 1224–1229. https://doi.org/10.1126/science.abe9985
- Kalluri, R., & LeBleu, V.S. (2020). The biology, function, and biomedical applications of exosomes. Science, 367(6478), eaau6977. https://doi.org/10.1126/science.aau6977
- Théry, C., et al. (2018). Minimal information for studies of extracellular vesicles 2018 (MISEV2018). Journal of Extracellular Vesicles, 7(1), 1535750. https://doi.org/10.1080/20013078.2018.1535750
- Horvath, S., & Raj, K. (2018). DNA methylation-based biomarkers and the epigenetic clock theory of ageing. Nature Reviews Genetics, 19(6), 371–384. https://doi.org/10.1038/s41576-018-0004-3
- Belsky, D.W., et al. (2020). DunedinPACE, a DNA methylation biomarker of the pace of aging. eLife, 11, e73420. https://doi.org/10.7554/eLife.73420
© 2026 XELGEN株式会社 · 〒160-0012 東京都新宿区南元町15-59
© 2026 XELGEN株式会社 · 〒160-0012 東京都新宿区南元町15-59, JAPAN