人が経験するあらゆる環境曝露——大気汚染、食事パターン、心理的ストレス、有害化学物質——はエピゲノムに分子的な痕跡を残します。遺伝子変異とは異なり、これらのエピジェネティックなマークは動的で可逆的、かつ累積的です。生涯にわたって蓄積され、身体が経験したすべての生物学的記録をエンコードします。XELGENのゲノムワイド850K CpGメチル化プラットフォームは、その歴史を臨床的解像度で読み取り——生涯にわたる環境シグナルを、医師と患者のための実用的な生物学的年齢インテリジェンスへと変換します。
はじめに:身体は記憶する
2025年2月、米国国立環境衛生科学研究所(NIEHS)のリック・ウォイチク所長がハーバード大学の疫学者アンドレア・バカレッリ教授と対談した際、議論の中心にあったのは一見シンプルな考え方でした——環境は単に健康に影響を与えるだけでなく、私たちの細胞に自らを書き込む、というものです。「環境は私たちの細胞に多くの指紋を残し、それを研究・分析することができます」とバカレッリ教授は説明しました。「私たちはDNAメチル化に焦点を当ててきました。これは細胞が過去の曝露の『記憶』を保持するシステムとして機能するエピジェネティック変化の一種です。」
この洞察は、生物学的老化の理解を根本的に変えます。暦年齢は生きた年数を数えます。生物学的年齢は、その年月をどのように生きたかの分子的結果——身体が処理したあらゆる曝露、ストレス、保護的または有害な環境シグナルの累積的な重み——を測定します。エクスポソームとは、受胎から死まですべての環境曝露の総体として定義されますが、これは抽象的な概念ではありません。ゲノム全体のメチル化マークとして書き込まれた物理的な記録であり、XELGENのプラットフォームはそれを読み取るために設計されています。
第I部:エクスポソームはいかにしてDNAメチル化に書き込まれるか
エピジェネティック記憶のメカニズム
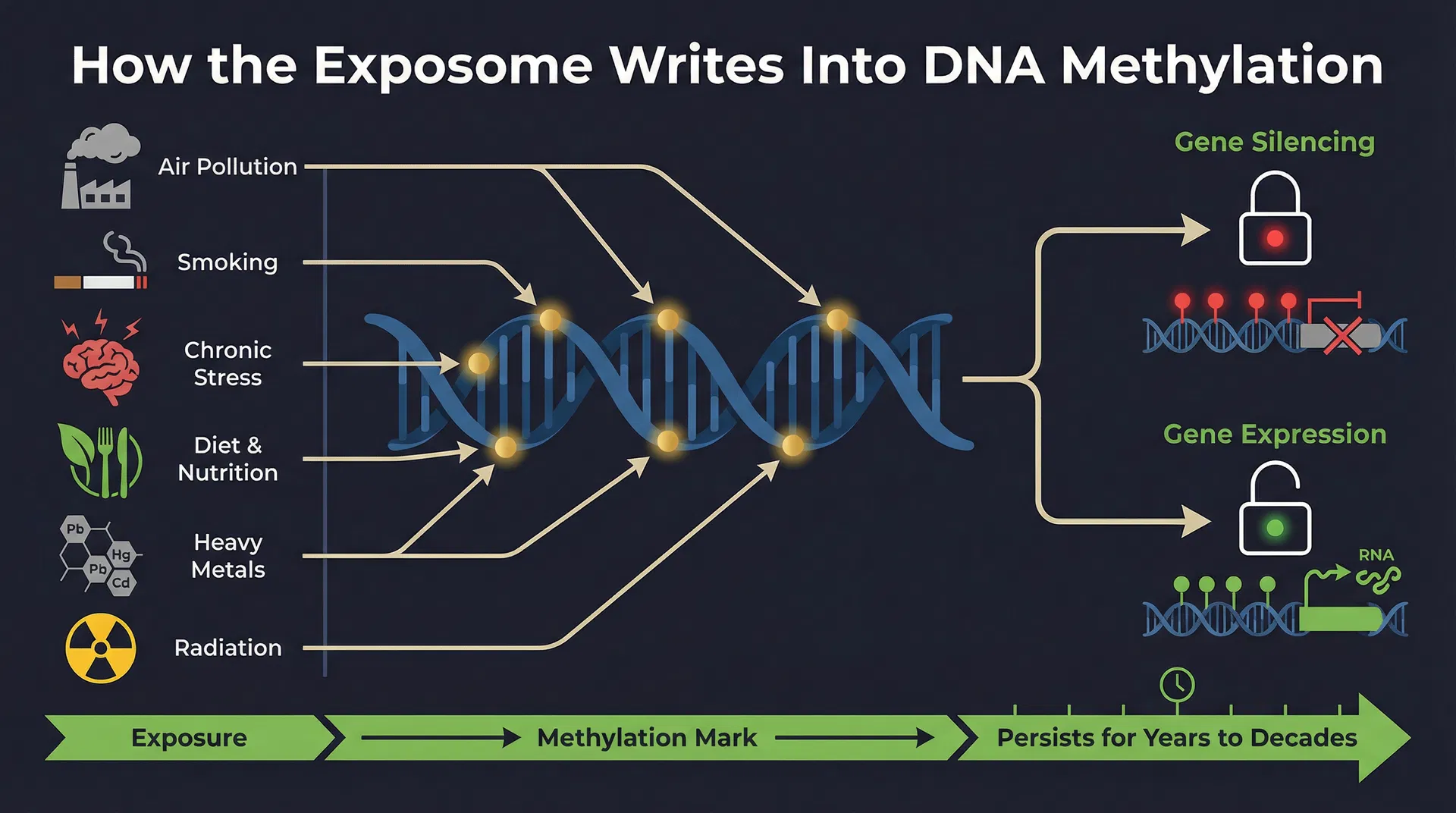
DNAメチル化は、CpGジヌクレオチドのシトシン塩基にメチル基(–CH₃)を付加することを指します。CpGサイトがメチル化されると、通常はそれに関連する遺伝子がサイレンシングされます。メチル化されていない場合、遺伝子は発現可能な状態にあります。このオン/オフの切り替えはランダムではなく、環境シグナルに応答する複雑な調節システムによって制御されており、その応答は持続的なマークを残します。
エクスポソーム研究からの重要な洞察は、環境曝露によって誘導されたメチル化変化の多くが、曝露が終了した後も何年、何十年、あるいは生涯にわたって持続するということです。バカレッリ教授の研究室は、メチル化データで訓練されたアルゴリズムが、曝露から何年も後に採取した血液サンプルから喫煙歴や過去の鉛曝露を特定できることを実証しています。この意味でエピゲノムは生物学的アーカイブとして機能します——身体の現在の状態だけでなく、その環境的歴史全体を記録する分子的日記です。
エクスポソームに含まれるもの
エクスポソームは広大です。化学的曝露(大気汚染物質、農薬、重金属、内分泌かく乱物質、PFAS化合物)、生物学的曝露(感染症、マイクロバイオーム組成、アレルゲン)、物理的曝露(放射線、温度、騒音)、心理社会的曝露(慢性的ストレス、社会経済的困難、トラウマ)を包含します。これらの曝露クラスはそれぞれ、ゲノム全体の特定のCpG座位に特徴的なメチル化シグネチャを残します。
| 曝露クラス | 代表的物質 | 主要メチル化標的 |
|---|---|---|
| 大気汚染 | PM2.5、NO₂、オゾン | FOXP3、iNOS、Alu反復配列 |
| 重金属 | 鉛、ヒ素、カドミウム | DNMT3A、CDKN2A、MLH1 |
| 残留性有機汚染物質 | PCB、ダイオキシン、PFAS | CYP1A1、LINE-1、APC |
| タバコ煙 | ニコチン、PAH、ニトロソアミン | AHRR、F2RL3、GPR15 |
| 心理的ストレス | コルチゾール、グルココルチコイド | NR3C1、FKBP5、SLC6A4 |
| 食事・栄養 | 葉酸、メチオニン、アルコール | IGF2、H19、PPARA |
| 身体活動 | 運動誘発シグナル | BDNF、PPARGC1A、TFAM |
第II部:XELGENの850K CpGプラットフォーム——記録を読む
ゲノムワイドメチル化解析のスケール
XELGENが使用するIllumina Infinium MethylationEPICアレイは、ヒトゲノム全体の850,000のCpGサイトを解析します。これはすべてのCpGサイトの約3%に相当しますが、最大の生物学的情報密度を提供するよう選択されています。このスケールにおいて、XELGENのプラットフォームは個々の曝露指紋だけでなく、生涯にわたる累積曝露の結果として生じた統合的なエピゲノム状態を捉えます。これは日記から一文を読むのと、本全体を読むことの違いです。
エピジェネティック時計:メチル化を生物学的年齢に変換する
| 時計 | 主要シグナル | 臨床的有用性 | エクスポソーム感度 |
|---|---|---|---|
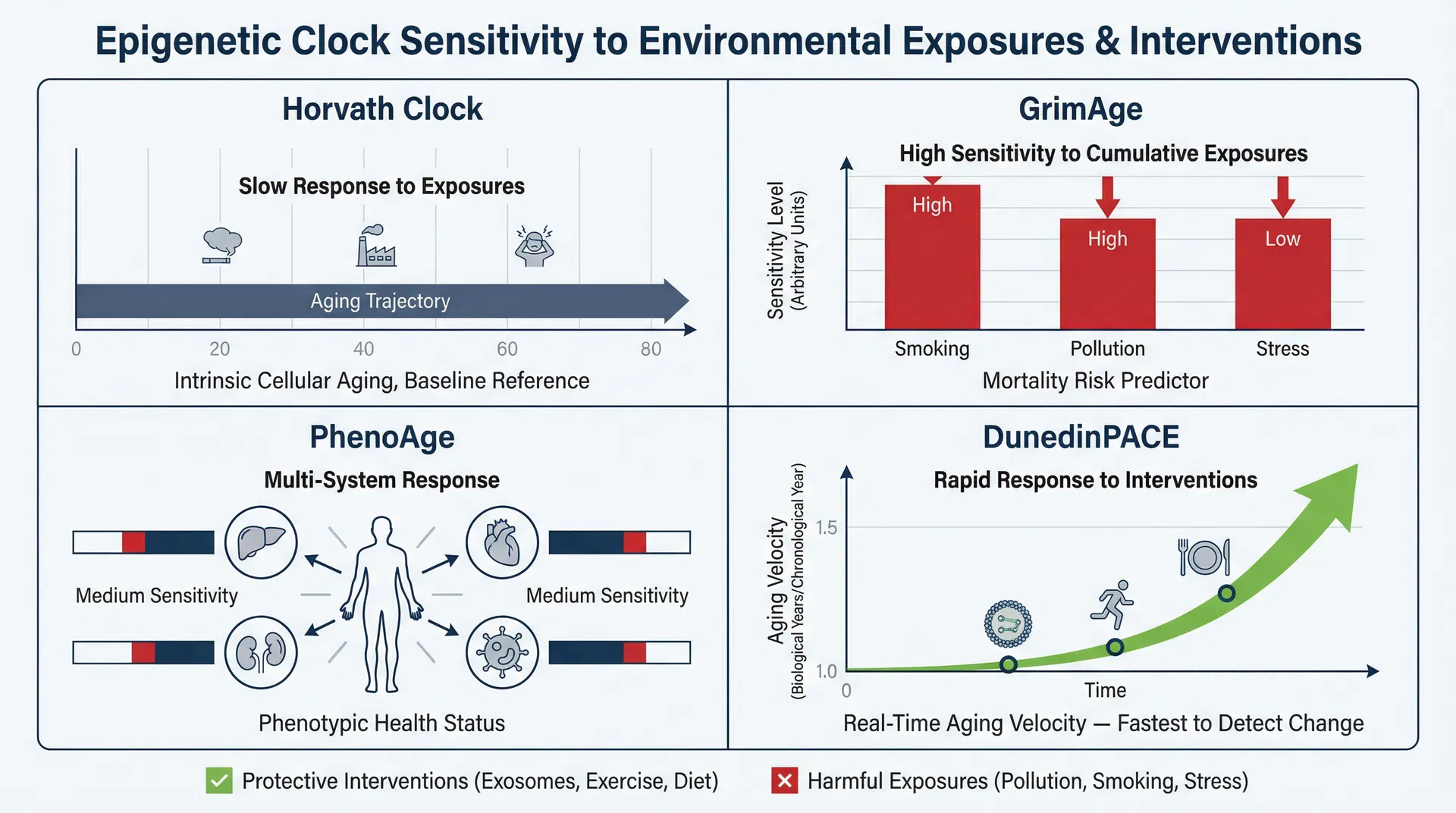
| Horvath時計(2013) | 内因性細胞老化 | 基準生物学的年齢 | 中程度 |
| GrimAge(2019) | 死亡率・疾患リスク | 累積曝露負荷 | 高 |
| PhenoAge(2018) | 表現型老化速度 | 多系統健康状態 | 高 |
| DunedinPACE(2022) | 現在の老化速度 | 介入モニタリング | 非常に高い |
第III部:エクスポソーム科学から臨床実践へ
検出タイムライン:エピゲノムはいつ応答するか
| 介入・変化 | 最初の検出可能シグナル | 有意な変化 | 最適時計 |
|---|---|---|---|
| 禁煙 | 4〜8週(AHRR座位) | 3〜6ヶ月(GrimAge) | GrimAge、DunedinPACE |
| 食事改善(地中海食) | 6〜12週 | 4〜6ヶ月 | PhenoAge、DunedinPACE |
| エクソソームIV療法 | 4〜6週 | 3〜4ヶ月 | 全時計 |
| 運動プログラム | 8〜12週 | 4〜6ヶ月 | DunedinPACE、PhenoAge |
| ストレス軽減 | 8〜12週 | 6〜12ヶ月 | GrimAge |
| NAD+補充 | 3〜4ヶ月 | 6〜10ヶ月(検出可能な場合) | DunedinPACE |
| 環境改善(汚染) | 3〜6ヶ月 | 12〜24ヶ月 | GrimAge |
XELGEN Cell Intelligence インサイト
このエピゲノムプロファイルは臨床歴に取って代わるものではなく、それを豊かにするものです。医師はメチル化データの分子的証拠に導かれながら、患者の職業歴、居住環境、過去の喫煙行動について的を絞った会話を行うことができます。介入の優先順位はそれに応じて設定できます——DunedinPACE 1.18が主に継続的なストレスと睡眠不足(FKBP5メチル化の上昇が示唆)によって駆動されている場合、それらの要因に対処することで最も速い測定可能なエピゲノム応答が得られます。
第IV部:XELGENモニタリングフレームワーク
基準エピゲノムプロファイル
4つすべての時計にわたる生物学的年齢、曝露特異的メチル化シグネチャ、および系統レベルの老化スコアを確立する包括的な850Kメチル化解析。これが患者の分子的出発点です。
介入設計
基準プロファイルに基づき、生物学的年齢加速の主要ドライバーとして特定された特定のメチル化シグネチャに導かれた標的介入プログラムを設計します。
早期応答モニタリング(3〜4ヶ月)
DunedinPACEとPhenoAgeに焦点を当てた850Kスクリーニングの繰り返し。このタイムポイントは介入への最初の検出可能なエピゲノム応答を捉えます。
転帰評価(6〜12ヶ月)
基準値との比較を含む完全な多時計解析。GrimAge加速がこの時点での主要転帰指標——1〜2年の減少は長期疾患リスクの臨床的に有意な改善を表します。
結論:臨床機器としてのエピゲノム
エクスポソームフレームワークは、XELGENが臨床的に行うことの明確な科学的根拠を確立します——生涯にわたる環境曝露がゲノムに書き込んだ分子的記録を読み取り、その記録を実用的な生物学的年齢インテリジェンスに変換し、それを書き換えるために設計された介入に対するエピゲノム応答を追跡します。
850K CpGプラットフォームは単なる生物学的年齢検査ではありません。精密環境健康のための臨床機器です——医師が反応的な疾患治療を超えて、積極的で個別化された生物学主導の予防へと移行するために必要な分子的証拠を提供します。長寿・再生医療クリニックを訪れるすべての患者は、生涯のエピゲノムアーカイブを携えています。XELGENの役割は、そのアーカイブを開き、その内容を読み取り、医師がその知識を活用して、残された生物学的に若い健康な年月を延ばすことを支援することです。
参考文献
Baccarelli, A.A. & Woychik, R. (2025). Epigenetics and the exposome: A new era of disease prevention. NIEHS Environmental Factor. www.niehs.nih.gov/news/factor/2025/2/feature/4-feature-epigenetics-and-the-exposome
Horvath, S. (2013). DNA methylation age of human tissues and cell types. Genome Biology, 14(10), R115. doi.org/10.1186/gb-2013-14-10-r115
Lu, A.T. et al. (2019). DNA methylation GrimAge strongly predicts lifespan and healthspan. Aging, 11(2), 303–327. doi.org/10.18632/aging.101684
Levine, M.E. et al. (2018). An epigenetic biomarker of aging for lifespan and healthspan. Aging, 10(4), 573–591. doi.org/10.18632/aging.101414
Belsky, D.W. et al. (2022). DunedinPACE, a DNA methylation biomarker of the pace of aging. eLife, 11, e73420. doi.org/10.7554/eLife.73420